Lambert-eaton Myasthenic综合征(LEMS)是一种罕见的自身免疫性疾病,影响美国10万人中的约1人。主要症状是肌肉弱点 - 自动抗体对电压门控钙通道的结果,导致从神经末端释放的乙酰胆碱(ACH)的量减少。1
LEMS最常见的临床介绍是近端肌肉弱点和易疲劳,可能导致行走和爬楼梯困难。古典三合会的lems包括近端腿部弱点,hymoreflex或arflexia,以及胆碱能脱血性病(干燥口,阳痿等)眼罩弱点是罕见的。当弱点涉及呼吸肌肉时,症状可能是危及的。大约50%-60%的LEMS患者具有潜在的恶性肿瘤,通常是小细胞肺癌(SCLC)。2-4
在lems中的氨米普啶
催化剂已完成FDA临床开发和担保FDA批准amifampridine.,神经元钾通道阻滞剂,用于治疗lems。
amifampridine.以前接受过FDA的孤儿药物指定和突破治疗指定。2018年,催化剂将NDA归因于LEMS中的Amifampridine使用。截至2018年11月,Amifampridine是唯一的基于FDA的FDA批准的成人患者患者患有兰伯特 - 伊顿肌腱综合症(LEMS)的诊断治疗。
第一个LEMS第3阶段试验(LMS-002)
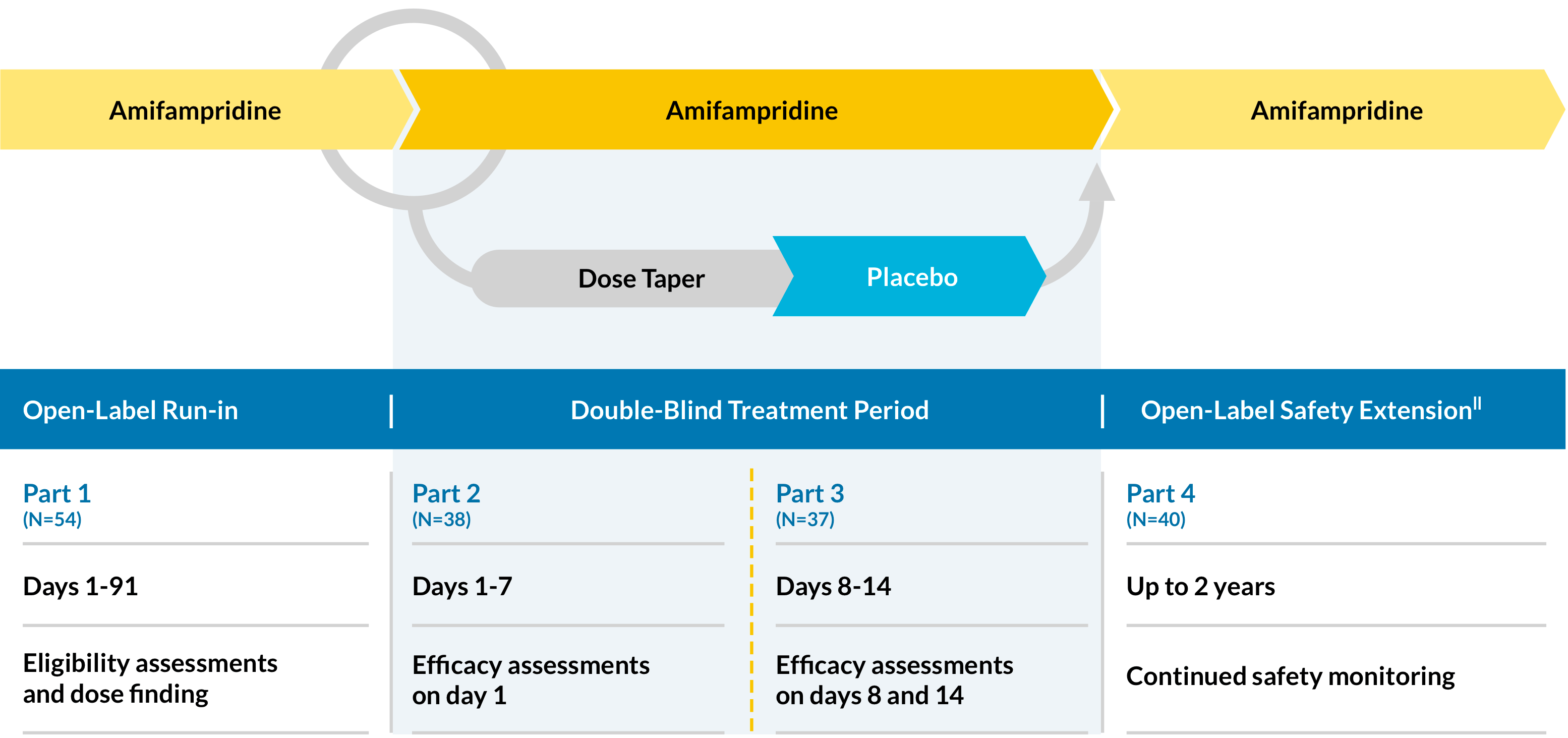
LMS-002是一个相3,多中心,双盲,安慰剂控制,随机化(1:1),中断研究,设计成4部分,以评估多剂量给药的功效和安全性amifampridine.患者患有lems。
功效措施
基本的:
- 从基线(第0天)到第14天的QMG得分*
- 改变SGI得分†从基线(第0天)到第14天
。
二次:
- 改变T25FW得分‡从基线(第0天)到第14天
- CGI-I分的变化§从基线(第0天)到第14天
安全评估
患者安全性不断评估,并且在2年的开放标签延伸期间进行剂量调整||
第二次LEMS第3阶段试验(LMS-003)
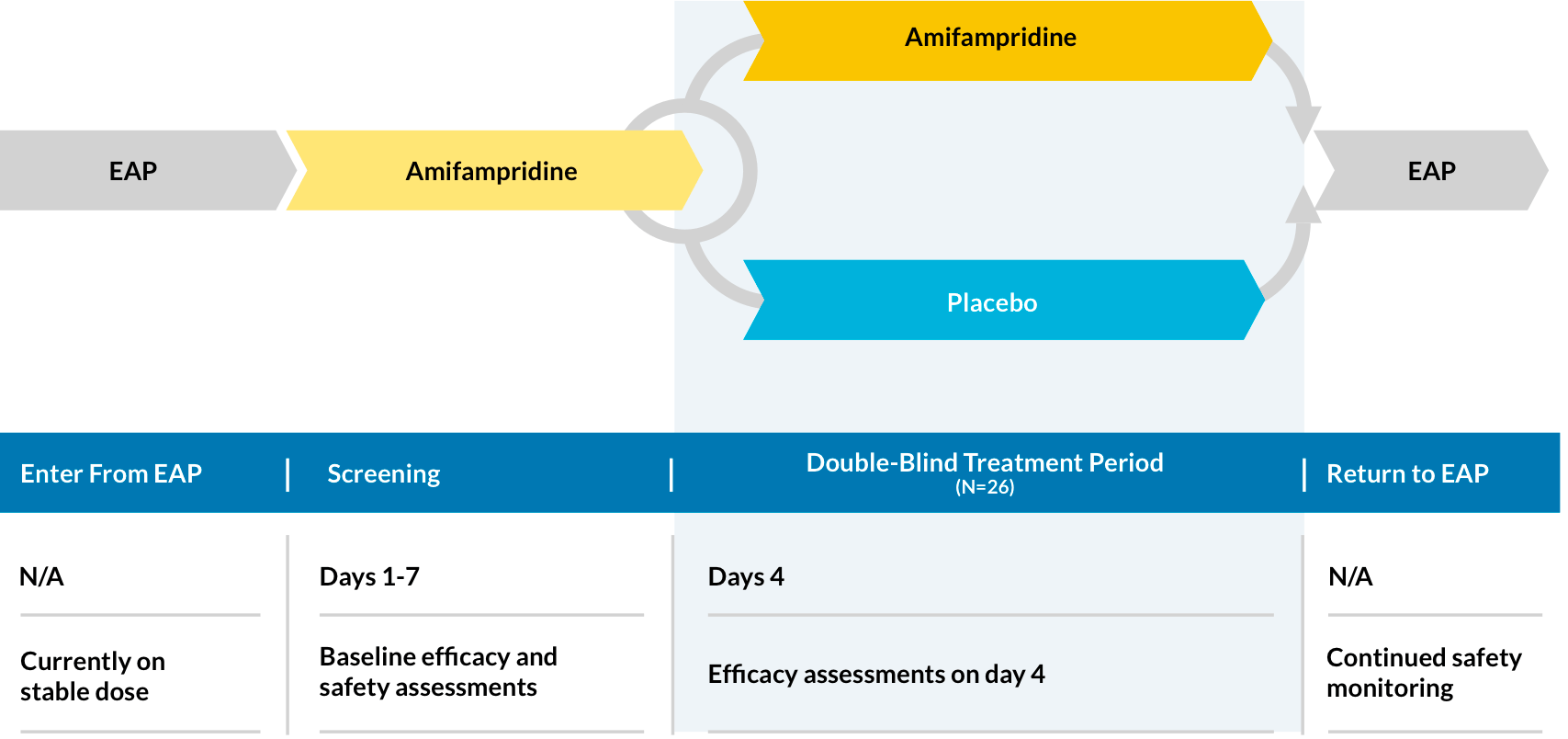
LMS-003是阶段3,双盲,安慰剂控制,随机(1:1),并行组研究,以评估疗效,安全性和效果磷酸氨氨酰胺患有lems患者的治疗。
功效措施
基本的:
- 从基线(第0天)到第4天结束的QMG得分*
- 改变SGI得分†从基线(第0天)到第4天结束
。
二次:
- CGI-I分的变化§从基线(第0天)到第4天结束
探索性:
- 在基线(第0天)时,三重时间上的变化(3tug)得分于第4天完成测试
安全评估
患者安全在筛选期和整个EAP中进行评估
CGI-I =临床全球印象 - 全球改进;EAP =扩展的访问程序;NDA =新药申请;qmg =定量myasthenia gravis;SGI =主题全球印象;t25fw =时间25英尺走。
- QMG是使用13评估的医生额定试验,包括面部强度,吞咽,握力,肢体可以保持在伸出的位置。13项中的每一个都被评分为0(无)到3(严重)。总分可以从0到39. QMG总分比与LEMS的恶化症状相关。
- SGI是一个受试者对整体福祉变化的感知的变化的衡量标准。要求患者使用7分尺度来评估其在前面的3天内的研究药物的影响的印象,在他们的身体健康上。7点SGI标准:1 =可怕;2 =大多不满意;3 =混合;4 =部分满意;5 =大多满足;6 =很高兴;7 =很高兴。
- T25FW试验是多发性硬化功能性复合材料的组分,是基于定时25英尺的步行(国家多发生硬化学会)的定量移动和腿功能性能测试。患者旨在尽可能快速,安全地在明显标记的25英尺的过程中行走。剩下的至少5分钟后,重复了25英尺的步行。患者可以使用辅助装置,例如罐头,拐杖或步行者。(所有数据都被标准化为每分钟的脚数,因此如果患者在不到一分钟的时间内走25英尺,则结果速度大于25英尺/分钟。T25FW测试的测量是平均速度,表达2个完成的散步的英尺/分钟。)
- The Investigator completed the 7-point CGI-I, based on changes in symptoms, behavior, and functional abilities, at the protocol-specified time points compared to the patient’s condition at day 0. The 7-point CGI-I scale: 1=very much improved; 2= much improved; 3=minimally improved; 4=no change; 5=minimally worse; 6=much worse; 7=very much worse.
- 在2年后续阶段(N-40)中,所有随机受试者和来自第1部分(第1-91天)的2个受试者继续进行。
参考:
- 哦,SJ,Shcherbakova N,Kostera-Pruszczyk A等;LEMS研究组Amifampridine磷酸盐(Firdapse®)在lems的3阶段临床试验中是有效和安全的。肌鼻子。2016; 53(5):717-725。
- orphanet。Lambert-eaton Myasthenic综合症。http://www.orpha.net/consor/cgi-bin/disease_search.php?lng=en&data_id=10583 &disease_disease_search_diseasegroup=lambert-eaton-myasthenic-syndrome&disease_disease_search_diseaseaseType=pat& disease (s)/(s)/goup%20of%20diseases=lagbert-eaton-myasthenic.-syndrome&title = lambert-eaton-myasthenic-syndrome&search = suestion_search_simple。进入2017年12月13日。
- Titulaer MJ,Lang B,Verschuuren JJ。Lambert-eaton Myasthenic综合征:从临床特征到治疗策略。柳狸神经酚。2011; 10(12):1098-1107
- 危害L,Sieb JP,Williams AE等。长期疾病史,临床症状,健康状况和医疗利用患者患有兰伯特伊顿骨髓综合征:德国患者面试调查结果。J Med Econ.。2012; 15(3):521-530。
Musk-Mg临床
SMA临床

现在有一个FDA批准的成人批准的一线治疗,具有lems的成年人。1,2
- 癫痫发作的历史
- 对氨基氨酰胺磷酸盐或另一种氨基吡啶的过敏率